El tejido muscular es responsable del movimiento de los órganos y de los organismos. Está formado por unas células denominadas miocitos o fibras musculares que tienen la capacidad de contraerse. El tejido muscular se divide en tres tipos: esquelético, cardiaco y liso.
1. Músculo esquelético estriado
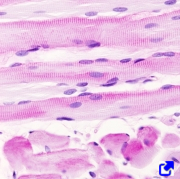
El músculo estriado esquelético se denomina también voluntario puesto que es capaz de producir movimientos conscientes. Está asociado principalmente al esqueleto a través de los tendones, aunque no siempre, como es el caso de la lengua. Está formado por células musculares estriadas esqueléticas, junto con tejido conectivo y vasos sanguíneos.
Las células musculares se asocian entre sí para formar los fascículos musculares, y éstos a su vez se unen para formar el músculo (Figura 1). Las células musculares están rodeadas por una lámina basal y por fibras reticulares y colágenas que forman el endomisio. Cada fascículo muscular está rodeado por otra envuelta de conectivo denso denominada perimisio, y todo el músculo por el epimisio, también tejido conectivo. Por estas envueltas de tejido conectivo penetran y se dispersan los vasos sanguíneos y ramificaciones nerviosas que controlan la contracción muscular.

Las células musculares estriadas se disponen en paralelo formando haces o láminas. Son células no ramificadas, muy largas y multinucleadas. El aspecto estriado se debe a la disposición especial del citoesqueleto. Aunque estas células pueden incrementar (hipertrofia) y disminuir su tamaño, no se suelen dividirse (hiperplasia) en condiciones normales.
No todas las fibras musculares son iguales sino que existen unas denominadas de contracción lenta y otras de contracción rápida. Las de contracción lenta actúan en movimientos prolongados y en el mantenimiento de la postura, mientras que las de contracción rápida actúan en movimientos breves e intensos.
2. Músculo cardiaco

El músculo cardiaco o miocardio forma las paredes del corazón. Su misión es el bombeo de sangre del corazón.
Sus células, los cardiomiocitos, son mayoritariamente mononucleados, cortos y ramificados, unidos entre sí por los discos denominados intercalares. Presentan estrías transversales cuyo patrón es similar al de las células musculares esqueléticas
La contracción rítmica del corazón está controlada por el sistema autónomo, por lo que también se le llama músculo estriado de contracción involuntaria. El ritmo se produce gracias a uniones en hendidura entre células contiguas, las cuales permiten la sincronía.
Músculo liso
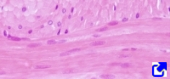
Al músculo liso también se le denomina involuntario o plano. Está formado por células fusiformes no ramificadas y cada célula sólo tiene un núcleo en posición central. El nombre de músculo liso se debe a que carece de estriaciones en su citoplasma. Se encuentra en todos aquellas estructuras corporales que no requieran movimientos voluntarios como el aparato digestivo, algunas glándulas, vasos sanguíneos, útero, etcétera.
Las células musculares lisas pueden aparecer aisladas en el tejido conectivo, formando haces muy pequeños en la dermis, unidos a los bulbos pilosos o formando láminas concéntricas en el aparato digestivo. El papel de la musculatura lisa en los órganos huecos es doble: mantener las dimensiones frente a expansiones potencialmente dañinas mediante su contracción tónica y realizar la función del propio órgano como el digestivo con los movimientos peristálticos o la regulación del flujo sanguíneo en el sistema cardiovascular.






